疑似rosuvastatin引起橫紋肌溶解症
橫紋肌溶解 (Rhabdomyolysis) 發生率低,約每10萬人年1.6件,1但可能有多數症狀輕微未被診斷而有所低估。造成的原因有很多,如直接肌肉受損、肌肉能量合成受損,透過外力、藥物、毒物、基因等,最終導致肌肉細胞壞死。其症狀從輕微的肌肉酸痛、虛弱、到急性腎衰竭、電解質失衡、心律不整或是瀰漫性血管內凝血(Disseminated Intravascular Coagulation, DIC)。趕緊停止可能的原因,並給予輸液、症狀治療與預防是很重要的。
案例簡介
L先生,95歲,身高172公分,體重50公斤。過去病史包括腎細胞癌、缺血性心臟病、感染性主動脈瘤、慢性阻塞性肺病、高血壓、高血脂,長期使用rosuvastatin
2.5 mg QD控制血脂。於111年6月6日開始使用voriconazole
200 mg Q12H治療肺部麴菌感染。6月28日,病人出現寒顫、冷汗、呼吸喘、有痰咳,懷疑肺炎及慢性阻塞性肺病急性惡化而住院治療。於急診時發現血中肌酸激酶 (Creatine kinase, CK又稱creatine
phosphokinase, CPK) 從最近一次5月22日的76 U/L增加至355
U/L,一路增加至6月29日的1677
U/L,肌球蛋白 (Myoglobin) 顯示1752
ng/mL,尿液呈琥珀色,將懷疑的rosuvastatin停用後,CK與myoglobin逐漸降低,7月5日分別降至正常值159U/L與68
ng/mL。
表一、病患住院用藥與相關檢驗值
|
藥名/含量/劑量/頻次 |
日期 途徑 |
5/ 22 |
06/ 27 |
6/28 05:23 |
6/28 12:59 |
29 |
30 |
07/ 02 |
05 |
|
Rosuvastatin FC |
PO |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
Voriconazole FC tab 200 mg 1# q12h |
PO |
|
|
|
|
|
|
|
|
|
從6/6 |
|
|
|
|
|
||||
|
Cefoperazone/sulbactam 2 g/vial 4g q12h
|
IV |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
Irbesartan FC tab 300 mg 0.5# qpm |
PO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Amlodipine tab 5 mg 0.5# q12h |
PO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
CK (39-308U/L) |
|
76 |
355 |
420 |
1041 |
1677 |
1018 |
544 |
159 |
|
Myoglobin |
|
|
|
1752 |
|
582 |
294 |
122 |
68 |
|
AST (<34 U/L) |
|
34 |
|
|
|
|
|
51 |
|
|
Creatinine (0.7-1.2 mg/dL) |
|
0.98 |
1.27 |
1.17 |
|
0.75 |
0.68 |
0.8 |
0.8 |
用藥評估與討論
一、橫紋肌溶解簡介2-4
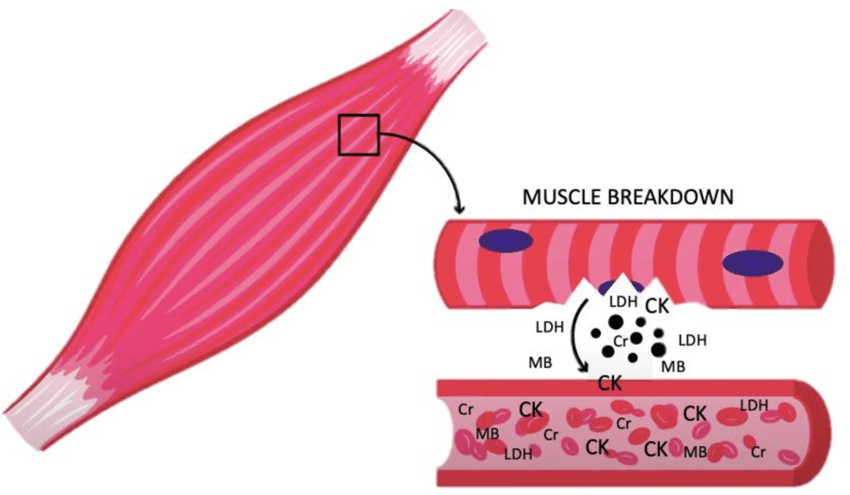
橫紋肌溶解一詞最早是由義大利醫師Antonino D’Antona於1908年西西里的美西納大地震(Messina earthquake)描述了受壓傷患者出現擠壓傷症候群 (crush syndrome) 引發的症狀。橫紋肌溶解定義為,肌肉組織破壞,細胞內容物流出進入血液循環,如CK、肌球蛋白、乳酸脫氫脢 (Lactate dehydrogenase, LDH)、醛縮酶 (aldolase)、天門冬氨酸轉氨酶 (aspartate transaminase, AST) 和丙氨酸轉氨酶 (alanine aminotransferase, ALT)、電解質,以及水分蓄積於肌肉內,而引發後續的問題。包括低血容
(hypovolemia)、急性腎衰竭 (acute kidney injury, AKI)、肌肉水腫疼痛、腔室症候群
(compartment syndrome)、肌球蛋白尿 (Myoglobinuria)、DIC、心律不整,從輕症到重症都有。
肌球蛋白在血中的半衰期很短,僅2-3小時,被腎臟排出或代謝成膽紅素 (bilirubin),約6-8小時幾乎全數消失。相比之下,CK半衰期1.5天,肌肉受損後約12小時開始上升,1-3天達到波峰,3-5天下降,所以臨床上主要使用CK來診斷橫紋肌溶解。CK正常值約為39 ~ 308 IU/L,沒有明確的上限,通常大於3-5倍 (約1000 IU/L) 便會開始懷疑橫紋肌溶解,但此時可能只有檢驗值異常,無明顯疼痛。當大於5000 IU/L則可能引發嚴重AKI,需要趕緊處理。
二、常見致病機轉
常見導致肌肉受損,甚至是橫紋肌溶解原因,可以粗分成3大類,肌肉過度運動、直接肌肉傷害與肌肉ATP不足。
(一)
過度運動:
n 平時沒做訓練,一下過度運動,如馬拉松、重訓…等,因而肌肉拉傷,又稱white-collars rhabdomyolysis (白領橫紋肌溶解)。特別是在大熱天,大量出汗導致低血溶,肌肉缺少血液供應氧氣,耗氧需求又高,肌肉壞死。網路上找到好幾篇paper都是初學者騎飛輪無站節(tsām-tsat),搞出來的。
n
癲癇重積狀態 (status epilepticus)、delirium (瞻望)、tremor (震顫) 導致肌肉過度抽搐。或是強烈抽筋也會使CK增加,若持續肌肉抽搐,則可能致病。
n
藥物、毒物、毒品導致肌肉過度抽搐而細胞損傷
i.
抗精神病藥物惡性症候群 (Neuroleptic malignant
syndrome, NMS): 抗精神病藥物與抗憂鬱藥物如Phenothiazine類藥物 (chlorpromazine,
prochlorperazine)、haloperidol、三環抗憂鬱劑、選擇性血清素再吸收抑制劑(Selective serotonin reuptake
inhibitors, SSRIs)…等,過度抑制中樞多巴胺受體,如抑制下視丘則造成高溫、自律神經失調;抑制黑質紋狀體造成類帕金森症狀、抖動、僵直;抑制脊髓造成僵直。也會促使周邊肌肉的鈣離子釋出,加重僵直症狀。另外,帕金森氏症患者長期使用的多巴胺補充劑,若突然停藥也可能引發NMS造成肌肉傷害。
ii.
血清素症候群 (Serotonin syndrome):SSRI、血清素-正腎上腺素再回收抑制劑 (Serotonin norepinephrine
Reuptake Inhibitors, SNRI)、Bupropion、三環抗憂鬱劑、單胺氧化酵素抑制劑 (Monoamine oxidase inhibitors, MAOIs)、抗偏頭痛藥物(carbamazepine、valproic acid、triptans)、嗎啡類藥物、鋰鹽、毒品 (麥角酸二乙醯胺(Lysergic acid
diethylamide, LSD)、搖頭丸 (Ecstasy)、古柯鹼(cocaine) 與安非他命 (amphetamines))、Linezolid、Ritonavir…等,劑量過高或合併使用,作用於5-HT1A與5-HT2A受體,可能出現高燒、肌肉過度抽搐。
iii.
惡性高熱 (Malignant hyperthermia):較常見於吸入性麻醉藥,如halothane、desflurane、enflurane、ether、isoflurane、sevoflurane或肌肉鬆弛劑如succinylcholine,可能透過抑制肌肉細胞的ryanodine 受體,造成肌肉過度抽搐、發燒、心跳過快等症狀。
iv.
毒品:Amphetamine、methylphenidate、cocaine、ketamine、MDMA、LSD…等活化交感神經肌肉過度收縮,加上血管收縮,供氧不足,壞死。
v.
毒物:在歐洲鵪鶉、知更鳥、燕雀等料理,該鳥類吃過毒參 (hemlock),其生物鹼對鳥類本身無害,但人吃了出現交感神經興奮、肌肉抽搐…等症狀。其他如中毒的小龍蝦、毒香菇也有類似情況。
(二)
直接傷害:
n 車禍、地震等造成擠壓傷症候群;臥床、昏迷等長時間壓迫導致肌肉損傷(尤其是肌肉缺氧超過2小時)。也可以是藥物如BZD、安眠藥、麻醉藥、鎮靜劑導致病人昏迷而長時間壓迫。橫紋肌溶解通常是發生於再灌流
(reperfusion) 之後,為了補償缺氧債,微血管通透性大增,水分隨著鈉離子紛紛流進肌肉組織,造成血管缺水,組織局部水腫,同時帶來大量的多核型白血球 (Polymorphonuclear leukocyte, PMN) 與前列腺素等發炎物質,產生自由基。進入細胞的鈣離子活化calcium
dependent phospholipase與protease進一步溶解細胞膜與促使肌細胞凋亡。
n
長期虐待、體罰之皮肉傷。
n
燒傷、炸傷、高壓電傷、雷擊直接破壞肌肉細胞
n
Daptomycin可能直接在肌肉細胞膜上開洞
脂蛋白抗生素Daptomycin,本身帶負電,透過結合鈣離子帶正電後結構改變 (conformation change),數個分子附著上細菌細胞膜,用他們長長的碳氫長鏈共同組成一個通道,讓細菌鉀離子不斷流失,膜電位下降,於是失去運動能力、部分對抗生素抗藥性、細胞合成與分裂與ATP合成酶的功能。但同樣的機轉也可能發生在人體的肌肉細胞膜上,產生破洞後,讓裡面的物質流出去。雖然發生率不高,但不建議與statin類併用,會讓肌肉細胞壞死的機率增加。
n
病毒 (influenza A&B、COVID-19、EBV、HSV)、細菌 (legionella、Group A streptococcus、staphylococcus、salmonella、clostridium toxins)、立克次體感染造成肌肉發炎、壞死
(三)
肌肉ATP不足:
n
一氧化碳中毒、休克、動脈阻塞、血栓、止血帶、極低溫導致血管收縮,皆可能造成組織缺氧ATP合成不足,肌肉壞死
n
Statin 抑制HMG-CoA reductase,結果連帶抑制了Coenzyme Q10合成,他是粒腺體有氧呼吸最後階段電子傳遞鏈中,負責傳遞電子的其中一個分子,缺少Q10則ATP無法合成,導致肌肉壞死。發生率約0.3-1.35/100萬 (但可能有許多症狀輕微而沒被診斷的黑數),5出現症狀的時間平均為用藥後第9天 (1到60天),若與fenofibrates併用,產生肌肉傷害的機率會更高。6
n
核苷酸反轉錄酶抑制劑(nucleoside
reverse-transcriptase inhibitors, NRTIs)Zidovudine可能抑制肌肉細胞粒線體DNA的合成,抑制ATP合成,造成肌肉壞死。
n
電解質失衡:
i. 低血鉀抑制肌肉肝醣分解,抑制血管擴張,減少肌肉細胞的供氧而死亡
ii. 低血磷缺乏ATP合成原料
iii. 低血鈉會造成肌肉組織水腫,也可能抑制Na-Ca pump而活化了protease與lipase去破壞肌肉細胞
iv. 高血鈉也有低機率產生橫紋肌溶解
n
酒精過量本身會傷害肌肉細胞,引起電解質失衡,喝到昏迷倒下而長時間壓迫,也會肌肉壞死。
n
H1 blocker:如Diphenhydramine過量可能導致癲癇、休克、體溫增加、昏迷而長時間壓迫,肌肉壞死。
n
遺傳代謝問題:
都是營養素的分解酵素出問題,最終無法產生ATP而肌肉壞死。
i. 糖解作用ATP合成的酵素缺乏:McArdle’s disease (myophosphorylase缺乏)、Tarui’s disease
(phosphofructokinase缺乏)、lactate dehydrogenase缺乏、粒線體respiratory chain enzyme缺乏
ii. 脂肪代謝酵素缺乏:carnitine palmitoyltransferase I &
II (CPT I&II) 缺乏
iii. 嘌呤代謝酵素缺乏:myoadenylate deaminase缺乏、Duchenne’s muscular
dystrophy
上述的各種原因,最終導致肌肉受損,細胞膜破裂,細胞外Na湧入細胞內,水分跟著滲透壓進入導致肌肉水腫,腔室症候群壓迫周邊肌肉組織連鎖死亡;初期表現低血鈣,因為大量細胞外鈣離子湧入細胞內,活化calcium dependent
phospholipase與protease進一步溶解細胞膜,並破壞Na-K-ATPase的作用,肌肉缺乏能量,於是壞死。肌肉內物質流入血中,造成高血鉀、高血磷(結合導致低血鈣),高尿酸血症 (核酸的嘌呤代謝)、高血鈣(後期)、DIC(thromboplastin流出)、AKI (肌球蛋白流出)…等症狀。
造成AKI的機轉
n
肌肉中釋出大量的肌球蛋白使尿液呈琥珀色,但不含紅血球。
n
在pH<5.6的尿中分解成具腎毒性的ferrihemate
n
其血基質 (heme) 上的亞鐵離子 (Fe2+) 氧化成鐵離子 (Fe3+) 產生具腎毒性的自由基,並促endothelin、TXA2、TNF-α、isoprostane釋放,與抑制NO的釋放,淨結果使腎血管收縮,血流減少
n
加上形成cast的globulin與尿酸結晶堵塞,使腎臟過濾率急性下降。
三、Rhabdomyolysis的處置原則7
1.
停止可疑藥品、症狀治療:若是藥物導致的橫紋肌溶解,應馬上停止可疑藥物。肌肉壓迫則改變姿勢或是進行筋膜切開。
2.
輸液改善循環:強力給水是所有治療手段中最重要,最有證據力的。盡早給予輸液避免hypovolemic
AKI,使用N/S或D5W 1L/hr輸注2hr,接著改以500 ml/hr輸注 (大部分trial給到3-4L/day),同時確保排尿量200-300
ml/hr,如此可以避免鬱血性心衰竭與肺水腫,同時也可以加速肌球蛋白的代謝,與防止腎小管內結晶。輸液直到CK降回正常值範圍,再開始慢慢減低劑量。
1、2為最重要處置,3、4不一定需要,不少trial光是給水就把病人CK打下來了,除非他腎功能在惡化、或尿不太出來。
3. 鹼化尿液:建議使用sodium bicarbonate使尿液pH值大於6.5、血液pH值不超過7.5,減少肌球蛋白分解成具腎毒性的ferrihemate,以減少沉澱與結晶的生成。也可避免N/S輸注而血液酸化、腎臟血管收縮,降低灌流量。可用劑量如1L 0.45% saline + 50mEq NaHCO3,再依臨床體液pH值調整劑量。若要用口服藥鹼化,則會吃12-24mEq(4-6#) Q4H
4.
利尿:如果病人可自行排尿就沒問題,但若你灌很多水,病人卻尿不出來。建議先裝上導尿管,且在病人至少還有尿量20 mL/hr時,可使用滲透壓性利尿劑20%
mannitol 50 mL泡於每1L輸液 (1-2 g/kg/day最多120 g) 流速5 g/hr來維持排尿量200-300 ml/hr,一方面減少肌肉內水分累積,降低腔室症候群風險。另一方面增加腎臟血液灌流,降低結晶沉澱生成,降低AKI風險。
但若病人已經寡尿或AKI則禁用mannitol,因為有血液高滲透壓、水分滯留的問題。一個簡單的測試,給予IV 20% mannitol 60ml 輸注3-5分鐘,若排尿量沒有比基礎值明顯增加30-50 mL/hr則不建議使用。若mannitol禁用或尚不足以維持足夠的排尿量,才考慮使用loop diuretics如furosemide,因為它有酸化尿液、低血鈣的風險。
5.
調整電解質:
n 高血鉀可使用regular
insulin + dextrose 50% + IV Na bicarbonate ± Calcium gluconate或Calcium
chloride、口服sodium polystyrene sulfonate螯合或furosemide來協助排出。並避免使用含鉀的Lacated Ringer輸液、高鉀的食物。
n 高血磷可使用利尿劑排出
n 低血鈣若嚴重或有出現症狀,則給予IV
Calcium gluconate或Calcium chloride
n 高尿酸血症
(Uric acid > 8 mg/dL)可使用allopurinol, febuxostat或benzbromarone
n 當體液過多排不出 (鬱血性心衰竭、肺水腫)、嚴重代謝性酸中毒、尿毒症、嚴重電解質過多,最後手段為洗腎,如血液透析 (hemodialysis)或連續性靜脈對靜脈血液過濾術 (Continuous venovenous hemofiltration, CVVH),但腹膜透析 (Peritoneal
Dialysis) 因為過濾效率較低,需要較長時間,對於急性電解質失衡較不適合。
結論
臨床上導致橫紋肌溶解的原因很多,從基因遺傳、外力傷害到藥物導致皆有可能,所幸真正導致嚴重症狀的比例不高。當發現病人CK增加超過5倍正常值時,則該調查可能的原因。在臨床上最常導致肌肉傷害或橫紋肌溶解的藥物為statin類降血脂藥,或是任何能影響意識造成久臥的藥物。盡早將可疑者停用,並且給予輸液、尿液鹼化、調整電解質,並留意腎功能的變化。留下紀錄後,應考慮有無其他能使用的替代藥物。
表二、導致橫紋肌溶解的藥物
|
可能機轉 |
藥名 |
|
肌肉過度抽搐 |
|
|
抗精神病藥物惡性症候群 |
抗精神病藥 抗憂鬱藥 如Phenothiazine類藥物
(chlorpromazine, prochlorperazine)、haloperidol、TCA
、SSRI 突然停止使用多巴胺補充劑 |
|
血清素症候群 |
抗憂鬱藥 如SSRI、SNRI、Bupropion、三環抗憂鬱劑、MAOIs 抗偏頭痛藥物如carbamazepine、valproic acid、triptans 嗎啡類藥物 鋰鹽 Linezolid Ritonavir 毒品如LSD、搖頭丸、古柯鹼與安非他命 |
|
惡性高熱 |
吸入性麻醉藥 如halothane、desflurane、enflurane、ether、isoflurane、sevoflurane 肌肉鬆弛劑如succinylcholine |
|
肌肉直接傷害 |
|
|
破壞細胞膜 |
Daptomycin |
|
活化過氧化物酶體增殖物活化受體α (Peroxisome proliferator-activated receptor
alpha)8 |
Fibrates 如gemfibrozil、fenofibrate |
|
昏迷久壓迫 |
H1
blocker、BZD、安眠藥、麻醉藥 |
|
肌肉ATP不足 |
|
|
抑制Q10 |
Statins、 |
|
抑制粒線體DNA的合成 |
NRTIs如Zidovudine |
參考資料
1.
Polyana Mendes, Priscila Games
Robles and Sunita Mathur. Statin-Induced Rhabdomyolysis: A Comprehensive Review
of Case Reports. Physiother
Can. 2014 Spring; 66(2): 124–132.
2. https://www.ncbi.nlm.nih.gov/books/NBK448168/?report=printable
3.
Efstratiadis G, Voulgaridou A,
Nikiforou D et al. Rhabdomyolysis updated. HIPPOKRATIA 2007, 11, 3: 129-137.
4.
Teresa J Coco 1, Ann E Klasner.
Drug-induced rhabdomyolysis. Curr
Opin Pediatr. 2004 Apr;16(2):206-10.
5.
Polyana Mendes, Priscila G Robles,
Sunita Mathur. Statin-induced rhabdomyolysis: a comprehensive review of case
reports. Physiother Can. 2014 Spring;66(2):124-32.
6.
Kandace
L Amend , Joan Landon, Veena Thyagarajan et al. Incidence of hospitalized
rhabdomyolysis with statin and fibrate use in an insured US population. Ann
Pharmacother. 2011 Oct;45(10):1230-9.
7.
Raymond Vanholder, MD, PhDMehmet S
Sever, MD. Crush-related acute kidney injury. UpToDate.
8.
Kazuya Kato, Astushi Nagase, Minoru
Matsuda et al. Rhabdomyolysis associated with fenofibrate monotherapy in a
patient with chronic myelogenous leukemia. Case Rep Gastroenterol. 2011
May;5(2):492-6.
沒有留言:
張貼留言